Sopesan inconvenientes de pausa
Panel de salud de EU insta a reiniciar aplicación de vacuna J&J
Beneficios superan riesgo poco común de coágulos de sangre; con información, ciudadanos podrán decidir por esta opción u otras
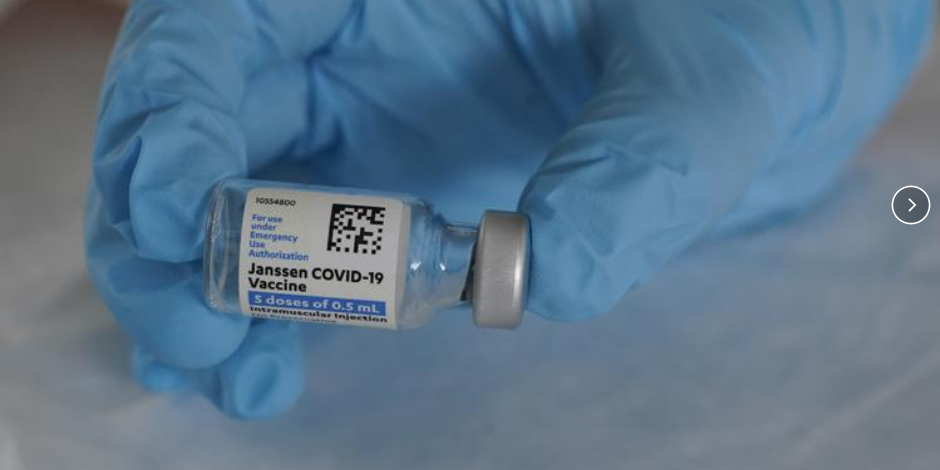
Asesores de salud de Estados Unidos instaron este viernes a reanudar las vacunas COVID-19 con la inyección de dosis única de Johnson & Johnson, diciendo que sus beneficios superan un riesgo poco común de coágulos de sangre, en línea con el lanzamiento en Europa.
Los funcionarios federales de salud descubrieron a 15 receptores de la vacuna que desarrollaron un tipo de coágulo de sangre muy inusual, de los casi 8 millones de personas que recibieron la vacuna J&J, todas eran mujeres, la mayoría menores de 50 años. Tres murieron y siete permanecen hospitalizadas.
Los asesores de los Centros para el Control y la Prevención de Enfermedades dijeron que si bien la vacuna de J&J es importante para combatir la pandemia, también es fundamental que se informe a las mujeres más jóvenes sobre ese riesgo en términos claros y comprensibles, para que puedan decidir si prefieren elegir una vacuna alternativa.
El panel votó 10 a 4 para levantar una pausa de 11 días en el uso de la inyección J&J y agregó advertencias que las mujeres y los trabajadores de la salud verían en los folletos en las clínicas de vacunación. El grupo debatió, pero finalmente se mantuvo alejado de las restricciones de edad absolutas.
“Este es un grupo de edad que está en mayor riesgo (de coagulación) que está recibiendo la vacuna principalmente para salvar la vida y la morbilidad de otras personas, no la suya propia. Y creo que tenemos la responsabilidad de asegurarnos de que ellos sepan esto”, dijo la Dra. Sarah Long de la Facultad de Medicina de la Universidad de Drexel, quien votó en contra de la propuesta porque sintió que no iba lo suficientemente lejos para advertir a las mujeres.
Los CDC y la Administración de Drogas y Alimentos sopesarán la recomendación del viernes al decidir si finalizar la pausa; el CDC normalmente sigue la recomendación de sus asesores y la directora de los CDC, la Dra. Rochelle Walensky, ha prometido una acción rápida.
Los reguladores europeos a principios de esta semana tomaron una decisión similar, decidiendo que el riesgo de coágulos era lo suficientemente pequeño como para permitir el lanzamiento de la inyección de J&J.
El problema es un tipo extraño de coágulo de sangre que se forma en lugares inusuales, como las venas que drenan sangre del cerebro, y en pacientes con niveles anormalmente bajos de plaquetas que forman coágulos. Los CDC y la Administración de Alimentos y Medicamentos detectaron inicialmente a seis personas que desarrollaron tales coágulos entre una y tres semanas después de la vacunación contra J&J. El viernes, los funcionarios de salud dijeron que nueve casos más salieron a la luz en la última semana.
Los informes de la aguja en un pajar despertaron la alarma porque los reguladores europeos ya habían descubierto coágulos raros similares entre los receptores de otra vacuna COVID-19, de AstraZeneca. Las tomas de AstraZeneca y J&J, aunque no son idénticas, están hechas con la misma tecnología.
Los científicos europeos encontraron pistas de que una respuesta inmune anormal que daña las plaquetas a la vacuna de AstraZeneca podría ser la culpable, y si es así, los médicos deberían evitar el tratamiento más común para los coágulos, un anticoagulante llamado heparina.
Con información de Associated Press
LRL
-
Survivor México 2024: ¿Quién es el eliminado de hoy 19 de abril?
-
¿Franco Escamilla le fue infiel a su esposa Gaby? Esta es la verdad
-
Eduin Caz reclama a banda en Mazatlán por cobrarle de más: '¿no que mucha feria?' (VIDEO)
-
Critican a Lucerito Mijares por cover de Adele: 'la única que le llega en México es Yuridia'
-
Resultados del Tris de hoy 19 de abril del 2024. Ve aquí los números ganadores

