La Organización Panamericana de la Salud (OPS) detectó “nudos críticos” en la Ley de Adquisiciones, para importar vacunas Covid-19 a México, a través de los Fondos Rotatorio de Vacunas (FRV) y Estratégico (FE).
En una nota técnica sobre barreras regulatorias sobre la compra de medicamentos de sistema público, consideró que la voluntad política de las máximas autoridades de México de avanzar en la materia requiere alinear el marco regulatorio.
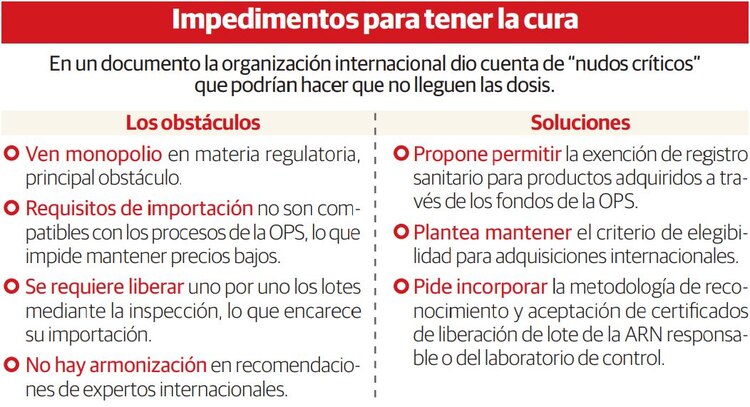
En cuanto a los requisitos de registro sanitario, la OPS consideró que existe un monopolio ya que el marco establece que los titulares del registro son los distribuidores exclusivos y es al que se le tiene que pagar, no al productor ni a la casa matriz.
“Este arreglo configura un monopolio y constituye el mayor obstáculo a la apertura del mercado. En la práctica hace inviable cualquier proceso de compra internacional y las ganancias en términos de ahorro que se podrían obtener”, expuso.
Además, planteó emitir un decreto ejecutivo que permita la exención de registro sanitario para productos adquiridos a través de los fondos de la OPS.
En criterios de elegibilidad para el ingreso de productos sin registro sanitario se incluye la precalificación de calidad de la Organización Mundial de la Salud (OMS) y la autorización de las Autoridades Reguladoras de Referencia (ARR) sólo para la primera importación, y para procesos posteriores el proveedor debe identificar un agente local que opera como titular.
“Estos requisitos no son compatibles con la OPS. La incorporación obligatoria de agentes intermediarios constituye una barrera importante de nuevos proveedores y encarece los costos, reduciendo la posibilidad de tener bajos precios”, indicó.
Por lo anterior, propuso mantener el criterio de elegibilidad, reconociendo la autorización de las ARR para la primera importación y para las subsecuentes.
Una tercera traba es el aval a la importación donde la Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) establece que el permiso requiere de la liberación de lotes mediante la inspección uno por uno al 100 por ciento, lo cual, argumentó, no es necesario para productos de compras internacionales.
Lo anterior, abundó, encarece el costo de importación, alarga el tiempo de autorización y podría hacer inviable la distribución de productos en el primer semestre de 2021. Por ello, propuso incorporar la metodología de reconocimiento y aceptación de certificados.
También identificó otro “nudo”, ya que el Compendio Nacional de Medicamentos contiene medicinas cuyas dosis no están armonizadas, lo que reduce la cantidad de proveedores y encarece el costo.
Y la última barrera es por medicamentos para enfermedades de rezago.

México, entre los países más afectados: OPS